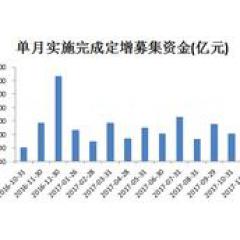
Yurt içinde üretilen ilk "anti-kanser ilacı" listeleme için başvurdu! Bu on milyarlarca piyasa değeri şirketi paniğe kapılıyor mu?

"Anti-kanser ilacı" son ilerlemeyi kaydetti.
13 Aralık'ta, Cinda Bio'nun monoklonal antikor enjeksiyonu "Sindi Mab", Eyalet Gıda ve İlaç İdaresi İlaç Merkezi tarafından kabul edildi ve pazarlanacak ilk yerel olarak üretilen PD-1 monoklonal antikor oldu.
Yeni Üçüncü Kurulda, 10 milyar yuan'ın üzerinde bir piyasa değerine sahip Junshi Bio (833330), PD-1 monoklonal antikor gelişimine de odaklanıyor. Uyuşturucular iyi olmasına rağmen rekabetin de aynı derecede şiddetli olduğu görülmektedir.
Listelenmek için uygulanan akran "anti-kanser ilacı"
"Sindimab" aynı zamanda yurtdışında Bristol-Myers Squibb (BMS) Opdivo'dan sonra Çin'de pazarlanan ikinci PD-1 / PD-L1 ilacıdır.
PD-1 / PD-L1 immünoterapi şu anda cerrahi, radyoterapi ve kemoterapi gibi yaygın tedavi yöntemlerine ve hedefe yönelik ilaç tedavisine ek olarak en son kanser tedavisidir.
Rolü, tümör hücreleri ve T hücrelerinin kombinasyonunu bloke etmektir, böylece "insan koruyucu" T hücreleri, insan vücudunda normal olarak işlev görebilir ve insan tümör hücrelerini belirleyip ortadan kaldırmaya devam edebilir. Bu nedenle PD-1 / PD-L1 ilaçları "anti-kanser ilaçları" olarak adlandırılır.
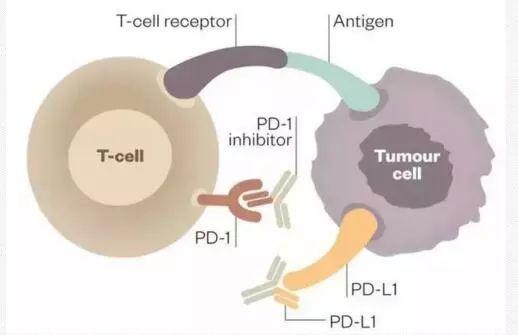
Sindizumab enjeksiyonu için başvuru endikasyonunun Hodgkin lenfoması olduğu bildirilmektedir. Bu endikasyona ek olarak, esas olarak ilerlemiş katı tümörlerin tedavisi için küçük hücreli dışı akciğer kanseri, özofagus kanseri ve NK / T hücreli lenfoma konusunda da klinik araştırmalara girmektedir.
13 Eylül 2016'da Sindimab, Devlet Gıda ve İlaç Dairesi tarafından klinik deneme için onaylandı.Mayıs 2017'de klinik aşama III'e girdi. Bugün, yarım yıl sonra, ürün pazarlama için başvurdu.
"Sindimab" ın klinik deneylerinin hızlı ilerlemesi, diğer yerli PD-1 / PD-L1 antikor araştırma ve geliştirme şirketlerini baskı hissettirmiş olabilir.
Şu anda dünya çapında piyasada 5 PD-1 / PD-L1 ilacı olduğu bildirilmektedir. Mevcut en çok satan PD-1 bağışıklık kontrol noktası inhibitörü olan Opdivo, 2015'te 942 milyon ABD Doları, 2016'da 3.774 milyar ABD Doları ve 2017'nin ilk üç çeyreğinde 3.587 milyar ABD Doları satış gerçekleştirdi.
Bazı analistler, endikasyonların sürekli artmasıyla, PD-1 antikor ilaçlarının satışının birkaç veya onlarca kat büyüme sağlayabileceğini tahmin ediyor.
Akranın "anti-kanser ilacı" listelenmek için başvuruda bulundu ve yeni üçüncü yönetim kurulu şirketi Junshi Biology de araştırma ve geliştirmeyi hızlandırıyor.
10 milyar piyasa değerine sahip "Katalizör"
Junshi Bio, 7 piyasa yapıcı ile yenilikçi bir kuruluştur. Ekim ayında, hisse senetlerinde güçlü bir artış dalgası vardı ve en son (24 Ekim) kapanış fiyatı 19.02 yuan idi Bu hesaplamaya göre, şirketin piyasa değeri 11.1 milyar yuan'a ulaştı.
Junshi Biotechnology'nin bu yılki hisse senedi fiyat grafiği:
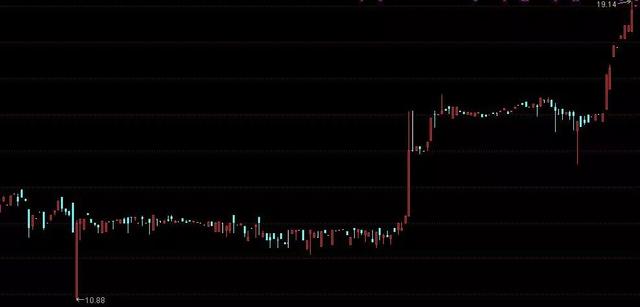
Yıllardır para kaybeden bu yeni ilaç araştırma ve geliştirme şirketi için yatırımcılar şüphesiz geliştirdiği "anti kanser ilacı".
Junshi Biology'nin son yıllardaki performansı:
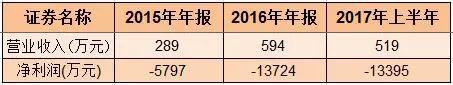
Junshi Bio'nun ana işi, araştırma altında olan ondan fazla çeşitle, monoklonal antikor ilaçlarının Ar-Ge'si ve sanayileştirilmesidir. Şirketin ilk yeni ilacı olan rekombinant insanlaştırılmış anti-PD-1 monoklonal antikor enjeksiyonu (JS001) şimdi faz II klinik denemelerine girdi.
Bu yılki altı aylık raporda şirket, JS001, UBP1211 ve diğer projelerin klinik denemelerini teşvik etmeye, sanayileşme sürecini hızlandırmaya ve JS001 ve UBP1211 projelerini mümkün olan en kısa sürede pazarlamaya çalışarak şirkete istikrarlı nakit akışı sağlamaya odaklandığını söyledi.
Sindizumab enjeksiyonunun endikasyonlarından farklı olarak, Junshi Biologics JS001 esas olarak melanom, ürotelyal kanser, mide kanseri, baş ve boyun kanseri ve akciğer kanseri gibi kötü huylu tümörlerin tedavisinde kullanılır.
Junshi Biosciences, 2015'te Yeni Üçüncü Kurul'da listelendiğinde, JS001'in 2016'da ilaç klinik denemeleri için onay alacağını ve ürünün 2020'de satışa çıkacağını umuyor. Aslında, Aralık 2015'te şirket ilacın klinik deneyleri için onay aldı.
2017 yılının ilk yarısında, faz I klinik araştırmalarının ardından şirket, melanom, ürotelyal kanser, mide kanseri, özofagus kanseri, baş ve boyun kanseri, nazofarengeal kanser ve diğer endikasyonlar için faz II klinik denemeler yapmaya başladı.
Junshi Biotech, listeleme sırasında JS001 şirketi ile aynı hedefe sahip ilaçların Merck'in Pembrolizumab ve Bristol-Myers Squibb's Nivolumab (Opdivo) olduğunu duyurdu. Bu iki ilaç 2014 yılında Amerika Birleşik Devletleri'nde piyasaya sürüldü.
Arıtma maliyetleri açısından Junshi Bio, rakip ürünler Opdivo ve Pembrolizumab'ın yıllık arıtma maliyetinin yaklaşık 150.000 ABD doları olduğuna ve JS001'in nispeten düşük işlem maliyetinin daha avantajlı olduğuna inanıyor.
Sermaye yatırımını artırın
Junshi Bio, rakip ürünler Opdivo ve Pembrolizumab'ın iç pazara girmesinin 3 ila 5 yıl alacağını belirtti. Her iki ilaç da 2014 yılında piyasaya sürüldü.
Son haberlere göre 2 Kasım'da Bristol-Myers Squibb, Çin'de PD-1 monoklonal antikor Opdivo'nun listelenmesi için başvuruda bulundu.
Analiz, Opdivo'nun önemli klinik faydaları olan yenilikçi bir ilaç olduğu göz önüne alındığında, AstraZeneca AZD9291'in Çin'de 2 aydan kısa süren onay hızına bakarsanız, Opdivo'nun 2018'in başlarında Eyalet Gıda ve İlaç Dairesi tarafından onaylanacağından çok umutlu olduğuna inanıyor.
Yerli Ar-Ge şirketleri açısından Hengrui Medicine, Junshi Bio gibi klinik deneme aşamasında olan JS001 ile aynı hedefe sahip ilaçlar geliştiriyor. Verilere göre, Hengrui Medicine'nin PD-1 ilacı olan camrelizumab klinik faz III'te ve kullanımları yemek borusu kanserini içeriyor.
Sindimab'ın hızına göre, Hengrui Medicine'nin PD-1 ilacının yakında listeleme başvurusu yapması bekleniyor.
Monoklonal antikor yenilikçi bir ilacın, temel araştırmadan ürünün pazarlama için onaylanmasına kadar sonuçları keşfetmesinin genellikle 10 yıl sürdüğü ve klinik öncesi araştırmadan pazarlamaya kadar genellikle 5-10 yıl sürdüğü bildirilmektedir.
Bununla birlikte, bazı araştırma verileri, faz II klinik çalışmalardan klinik faz III'e kadar yeni ilaçların başarısız olma riski olabileceğini göstermektedir.
Junshi Biotech ayrıca, şirket tarafından tasarlanan klinik araştırma programının Devlet Gıda ve İlaç İdaresi'nin ilgili düzenlemelerine uygun olmasına ve profesyonel ve istatistiksel tasarım gerekliliklerini karşılamasına rağmen, faz II ve III klinik araştırmalardaki daha karmaşık ve artan belirsizlikler nedeniyle, Bununla birlikte, klinik araştırma programının uygulama etkisi yine de beklenenden düşük olabilir.
Sektör uzmanlarına göre, klinik aşama III'ten listeleme onayına kadar yaklaşık üç yıl sürüyor. Bu, JS001 ürününün planlandığı gibi 2020'de pazarda tanıtılması için Junshi Bio'nun ilacın geliştirilmesini hızlandırması gerektiği anlamına gelir.
Yeni ilaç yatırımı uzun süre, yüksek risk ve aşamalı olarak önemli sermaye gereksinimi özelliklerine sahiptir Sermaye yatırımı tüm Ar-Ge sürecinden geçer ve yüz milyonlarca fon gerektirir.
16 Ekim'de askıya alınmadan önce, Junshi Biotechnology, JS001 klinik deneme projesine yatırım yapmak için 200 milyon yuan kullanmayı planlayan 500 milyon yuan çift teşebbüs dönüştürülebilir tahvil halka arzını başlattı. Bu projede toplam planlanan yatırımın 1 milyar yuan olduğu bildirildi.
Şirkete göre 200 milyon yuan, melanom, nazofaringeal karsinom, mesane ürotelyal kanseri, üçlü negatif meme kanseri, renal hücreli karsinom, mide kanseri, özofagus skuamöz hücre karsinomu ve baş ve boyun skuamöz hücreli karsinomu içeren faz II endikasyonları için kullanılacak. , JS001 listelemesinin hızını artırmak için Faz III klinik denemeler.
Ayrıca, Junshi Bio 13 Aralık'ta 2015'ten 2016'ya kadar üç sabit artışın, JS001 klinik araştırma ve sanayileşme temel projelerine yatırımı artırmak için toplanan fonların bir kısmının JS001 listelemesini hızlandırmak amacıyla kullanımını değiştireceğini duyurdu. hız.
Ekstra! ! ~~
En sıcak NEEQ şirketini bilmek ister misiniz?
Yeni Üçüncü Kurul'un çeşitli okullarından Huashan ile kılıçları tartışmak ister misiniz?
Çin'in Nasdaq'ında servet özgürlüğünü gerçekleştirmek ister misiniz?
WeChat Kimliği eklemek için aşağıdaki QR kodunu basılı tutun sbxxxsb2
Sizi "Yeni Üçüncü Kurul Forum Değişim Grubu" na çeker
·SON·
Yeni Üçüncü Kurul Forumu
En değerli orijinal yenilikçi üç kartlı mikro sinyal
Bizi takip etmek için yukarıdaki QR koduna uzun basın
WeChat Kimliği: zqsbxsb
-

- Liu Xiaoqing, kayıt stüdyosunda yeniden ortaya çıktı ve resim geri çekilebilir görünüyordu, ama aslında ayak parmağı o kadar gergindi ki canını yaktı!
-

- Bir tarafta 11 ana oyuncu ortaya çıktı, 3 yabancı yardım + 8 büyük uluslararası oyuncu, toplam değeri 400 milyonu aştı
-

- Filmdeki film müziği ve özel efektler nasıl tamamlanır? "Tekrar tekrar sürpriz" cevabı sizin için ortaya koyuyor!
-

- Yang Mi'nin ailesinin çocukluk fotoğraflarını sayan Hawick Lau, yakışıklı olmaktan çıkıp büyümüş ve Xiao Nuomi daha da sevimli.
-

- Resmi duyuru! Yanbian Fude resmen iflas etti ve feshedildi ve 3 yıl içinde ikinci olmayı hedefleyerek şampiyonaya katılmak için bir takım oluşturacak
-

- Yağsız ve susuz lezzetli yapabilir misin? Nasıl besleyici ve sağlıklı sarı şarlatan yapılacağını öğretin